CBSE Gujarat Board Haryana Board
Class 10 Class 12
ધાતુની પાણી સાથેની પ્રક્રિયાઓ લખો. અથવા હાઈડ્રોજન વાયુની બનાવટનાં સમીકરણો લખો.
H2, C, O, S નો ઉપયોગ લખો.
એમોનિયા વાયુના રસાયણિક ગુણધર્મો નીચે પ્રમાણે છે :
(1) હાઈડ્રોજન ક્લોરાઈડ વાયુ સાથે પ્રક્રિયા : એમોનિયા વાયુની હાઈડ્રોજન ક્લોરાઈડ વાયુ સાથે પ્રક્રિયા થતાં ઘન એમોનિયા ક્લોરાઈડ મળે છે.
દા. ત., NH3(g)+HCl(g)→NH4Cl(s)
(2) એમોનિયાની રિડક્શનકર્તા અસર : ગરમ ક્યુપ્રિક ઑક્સાઈડ (CuO) પરથી એમોનિયા વાયુ પસાર કરતાં કાળા રંગના ઑક્સાઈડનું રિડક્શન થઈ લાલ કથ્થાઈ રંગની કૉપર ધાતુ મળે છે.
દા. ત., 2NH3(g)→3Cu(s)+3H2O(1)+N2(g)
(3) એમોનિયાનું ઉદ્દીપકીય ઑક્સિડેશન અથવા ટૂંક નોંધ : ઓસ્વાલ્ડ પદ્વતિ : એમોનિયા અને ડાયઑક્સિજન વાયુના મિશ્રણને 1073 K તાપમાને ગરમ કરેલ પ્લેટિનમ ઉદ્દીપક પરથી પસાર કરતાં એમોનિયા વાયુનું નાઈટ્રિક ઑક્સાઈડમાં ઑક્સિડેશન થાય છે.
4NH3(g)+5O2(g)→4NO(g)+6H2O(g)
ઉત્પન્ન થતો નાઈટ્રિક ઑક્સાઈડ તરત જ ઑક્સિજન સાથે સંયોજાઈ નાઈટ્રોજન ડાયૉક્સાઈડના કથ્થાઈ રંગના ધુમાડા આપે છે.
2NO(g)+O2(g)→2NO2(g)
આ નાઈટ્રોજન ડાયૉક્સાઈડ પાણી સાથે પ્રક્રિયા કરી નાઈટ્રિક ઍસિડ બનાવે છે.
3No2(g)+H2O(1)→2HNO3(aq)+NO(g)
આમ, એમોનિયા વાયુમાંથી નાઈટ્રિક ઍસિડ મેળવવાની આ પદ્વતિ ઓસ્વાલ્ડ પદ્વતિ તરીકે ઓળખાય છે.
(4) એમોનિયા વાયુની લિટમસપત્ર પર અસર : શુષ્ક એમોનિયા વાયુ ભીના લિટમસપત્ર પર અસર બતાવતું નથી, પરંતુ એમોનિયાનું જલીય દ્રાવણ નિર્બળ બેઝિક હોવાથી તે લાલ લિટમસપત્રને ભૂરું બનાવે છે.
એમોનિયા વાયુ પાણીમાં દ્રાવ્ય થઈને નિર્બળ બેઈઝ એમોનિયમ હાઈડ્રૉક્સાઈડ બનાવે છે. જેનું અલ્પ પ્રમાણમાં આયનીકરણ થઈ OH-મળે છે.
દા. ત., NH3(g)+H2O(1)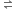 NH4OH(aq)
NH4OH(aq)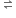 NH4+(aq)+OH-(aq)
NH4+(aq)+OH-(aq)
NH4OH બેઝિક હોવાથી તે હાઈડ્રોક્લોરિક ઍસિડ સાથેની પ્રક્રિયાથી એમોનિયમ ક્લોરાઈડ (ક્ષાર) અને પાણી બને છે. દા. ત., NH4OH(aq)+HCl(aq)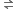 NH4Cl(aq)+H2O(1)
NH4Cl(aq)+H2O(1)
(5) ધાતુ આયન સાથે પ્રક્રિયા : એમોનિયાના જલીય દ્રાવણની ધાતુ આયનના ક્ષારના જલીય દ્રાવણ સાથે પ્રક્રિયા થવાથી પાણીમાં અદ્રાવ્ય ધાતુ હાઈડ્રૉક્સાઈડ બને છે.
દા. ત., ક્યુપ્રિક સલ્ફેટના જલીય દ્રાવણમાં એમોનિયમ હાઈડ્રૉક્સાઅઈડનું દ્રાવણ ઉમેરતાં ભૂરા રંગના ક્યુપ્રિક હાઈડ્રૉક્સાઈડના અવક્ષેપ મળે છે.
CuSO4(aq)+2NH4OH(aq)→Cu(OH)2(s)+(NH4)2SO4(aq)
Cu(OH)2 ના અવક્ષેપમાં વધુ પ્રમાણમાં NH4OH ઉમેરતાં અવક્ષેપ દ્રાવ્ય થઈ ઘેરા ભૂરા રંગનું દ્રાવણ મળે છે, જે કૉપરના એમોનિયા સાથેના બનતા સંકીર્ણ ક્ષારને કારણે હોય છે. દા. ત., Cu(OH)2(s)+4NH4OH(aq)→[Cu(NH3)4](OH)2(aq)+4H2O(1)
આ જ પ્રમાણે ફેરસ સલ્ફેટ, મૅગ્નેશિયમ સલ્ફેટ અને ઍલ્યુમિનિયમ ક્લોરાઈડ સાથે NH4OH અનુક્રમે ફેરસ હાઈડ્રોક્સાઈડ, મૅગ્નેશિયમ હાઈડ્રોક્સાઈડ અને ઍલ્યુમિનિયમ હાઈડ્રૉક્સાઈડ બનાવે છે.
દા. ત., FeSO4(aq)+2NH4OH(aq)→Fe(OH)2(s)+(NH4)2SO4(aq)
MgSO4(aq)+2NH4OH(aq)→Mg(OH)2(s)+(NH4)2SO(aq)
AlCl3(aq)+3NH4OH(aq)→Al(OH)3(s)+3NH4Cl(aq)
સમજાવો :
હાઈડ્રોજન